Virus chřipky – struktura a molekulární biologie
Viry chřipky, které jsou původci závažných infekčních onemocnění lidí a zvířat, provází lidstvo od počátků civilizace. Na jedné straně jsou významným patogenem, který má závažný zdravotní a tudíž ekonomický dopad, na druhé straně je to významný faktor přírodního výběru v živočišné říši.
Závažnost chřipkových onemocnění lze demonstrovat na počtu vědeckých prací, které se chřipkou zabývají. Do roku 2019 bylo publikováno 67123 prací s tématem chřipky, z čehož 9402 prací se týkalo vakcín. Struktura viru chřipky je na obrázku 1. Segmentovaný genom na bázi RNA je důvodem pro rychlý vznik variant virů na základě mutace (antigenní drift) a výměny segmentů RNA (antigenní schift) za vzniku reasortovaných virů. Zejména antigeny odvozené od neuraminidázy a hemaglutininu jsou klíčovými komponentami vakcín proti chřipce.
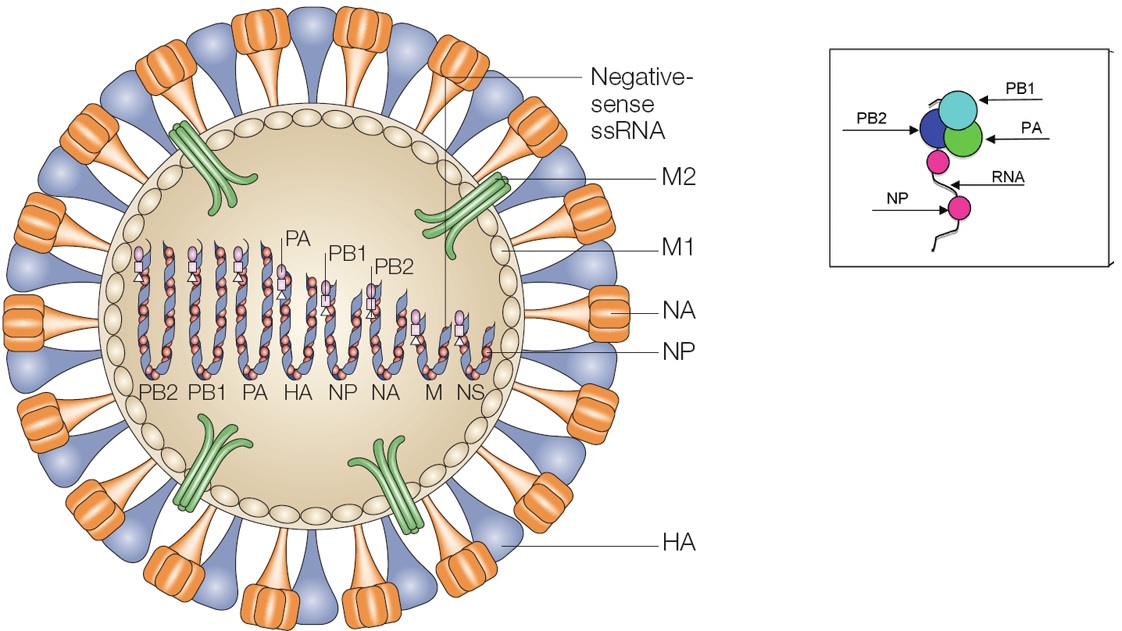
Obr. 1 Struktura viru chřipky typu A.
Dva povrchové glykoproteiny, hemaglutinin (HA) a neuraminidáza (NA), a protein iontového kanálu M2 jsou zabudovány do virové obálky, která je odvozena z plazmatické membrány hostitele. Ribonukleoproteinový komplex obsahuje virový RNA segment spojený s nukleoproteinem (NP) a tři polymerázové proteiny (PA, PB1 a PB2). Matricový (M1) protein je spojen jak s ribonukleoproteinem, tak s virovým obalem. (https://www.nature.com/scitable/topicpage/genetics-of-the-influenza-virus-716/). Protilátková odpověď na virus chřipky A se typicky zaměřuje na povrchové glykoproteiny HA a NA, zatímco odpověď zprostředkovaná T-buňkami se typicky zaměřuje na relativně konzervované interní proteiny včetně NP, M1 a PB1. Upraveno podle Emma J. et al. T-Cell Immunity to Influenza A Viruses. Critical Reviews™ in Immunology, 2014, 34(1),15–39); Vincent AL et al. Influenza A virus vaccines for swine. Veterinary Microbiology 2017, 206 35–44.
Obranné mechanismy při infekci virem chřipky
Imunitní odezva vůči virům je složitý proces zahrnující jak vrozenou, tak adaptivní imunitní odpověď na infekci viry. Humorální a buněčně zprostředkovaná imunita namířená proti infekci virem chřipky je základem pro eliminaci infekce. Respirační trakt představuje zvláštní výzvu pro imunitní odpověd, protože zánětlivá reakce musí na jedné straně být dostatečně silná, aby eliminovala virus, ale musí být na druhé straně minimalizováno poškození tkání respiračního systému, neboť by to vedlo k selhání funkce plic a závažným zdravotním následkům, které končí smrtí. Podíl vrozené a adaptivní imunity na obranné reakci proti viru chřipky je sumarizován na obrázku 2.
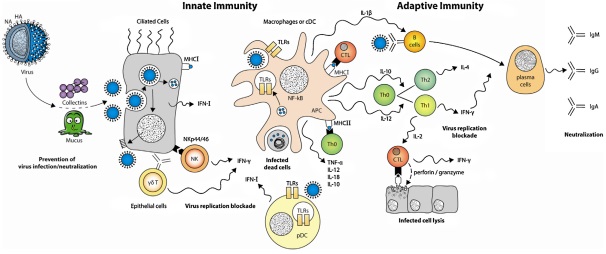
Obr. 2 Imunita během infekce virem chřipky. Vrozený imunitní systém tvoří první linii obrany proti chřipkové infekci. Skládá se z množství komponent, jako jsou hlen, kolektiny a proteiny akutní fáze, jejichž cílem je zabránit infekci epiteliálních buněk respiračního traktu. Další linii obrany tvoří buňky přirozené imunity, jako jsou makrofágy, dendritické buňky, NK-buňky a γδT buňky s cílem kontrolovat a blokovat replikaci a šíření viru v organismu a organizovat následnou adaptivní imunitní odpověď pomocí vylučování různých typů chemických mediátorů, jako jsou cytokiny, které aktivují T buňky a indukují jejich diferenciaci nebo vyvolávají adaptivní odpověď s produkcí specifických protilátek, které neutralizují virus a brání jeho přechodu přes sliznici (obrázek použit z publikace: Crisci E et al. Influenza virus in pigs. Molecular Immunology 2013, 55, 200– 211).
Typy vakcín proti chřipce
Využití antivirotik pro chemoterapii chřipky je doposud nedořešena a pro veterinární aplikace, zejména v chove hospodářských zvířat, je tento přístup nepoužitelný z hlediska ekonomického.
Aplikace vakcín a hygienických opatření je tedy v současnosti jediným způsobem, jak lze čelit chřipkovým infekcím lidí a zvířat. Vývoj vakcín proti chřipce zahrnuje všechny přístupy využívané ve výrobě vakcín. Současné dostupné vakcíny i vakcíny ve vývoji jsou založeny na živých atenuovaných vakcínách, inaktivovaných vakcínách, splitovaných vakcínách, rekombinantních vakcínách a ve vývoji jsou vakcíny genové, které využívají konstrukty na bázi mRNA nebo pDNA. Zejména genové vakcíny představují potenciální průlom v oblasti vývoje vakcín pro použití jak v humánní, tak veterinární medicíně.
Inaktivované vakcíny
Jedná se o nejstarší typ vakcín, které byly poprvé licencovány v USA v roce 1943. Strukturně se jedná o celé viriony chřipkového viru, které byly produkovány v kuřecích embryích, purifikovány zonální centrifugací a inaktivovány formaldehydem. Faktorem, který ovlivňoval bezpečnost, byly kontaminující komponenty z kuřecích embryí, které byly odstraňovány purifikačními technologiemi a snaha o potlačení reakcí na vakcinace vedla k vývoji splitovaných a subjednotkových vakcín. Tyto vakcíny jsou založeny na solubilizaci virionu detergenty a odstranění virové RNA spolu s dalšími komponentami virionu. Převažujícími antigeny z virionu tak zůstávají hemaglutinin a neuraminidáza, jako dva zásadní antigeny pro navození imunitní odpovědi. Tento typ vakcín je třeba formulovat s adjuvans. Tyto vakcíny jsou obecně dobře tolerovány. Nejčastějším vedlejším závažným účinekem při podání lidem je bolestivost v místě aplikace a riziko vzniku akutní zánětlivé demyelinizační polyneuropatie (Guillan-Barré syndrom).
Živé atenuované vakcíny
V těchto vakcínách jsou využívány viry chřipky, které jsou adaptovány na replikaci při 25°C s omezenou replikací při 38-39°C. Proces chladové adaptace je založen na postupném snižování teploty, při které se virus replikuje a izolaci mutantů, adaptovaných na replikaci při chladu. Replikace těchto mutovaných virů je nejméně o dva řády nižší při teplotách fyziologických teplotám savců. Výhodou takových vakcín je navození protektivní imunitní odpovědi jako při přirozené infekci. Zároveň není třeba formulovat vakcínu s adjuvans a vakcína je podávána na sliznice, nikoliv injekčně. Z hlediska veterinárního použití je možno aplikovat vakcínu rozprašováním (drůbež), nebo intranasálně. Multivalentní vakcíny, které obsahují různé atenuované kmeny chřipkových virů, umožňují indukci širší imunitní odpovědi. Je navozena jak systémová, tak mukózní imunitní odpověď s dobou trvání kolem jednoho roku. U těchto vakcín je ovšem doprovodným jevem šíření virů z vakcinovaných jedinců do prostředí, což sebou nese určité potenciální riziko. Analýza takto šířených virů prokázala uchování atenuovaného fenotypu a genotypu.
Technologie výroby výše uvedených vakcín je založena na produkci virů v embryích slepičích kuřat, což má své limity v kapacitě produkce vakcín a v purifikaci viru. Další limitací je doba vývoje a produkce dostatečného počtu dávek, zejména s ohledem na sezónnost chřipky a antigenní variabilitu danou antigenním driftem a shiftem. Rychlost vývoje a výroby vakcín je klíčovým parametrem pro úspěšnost vakcinační kampaně vzhledem k epidemickému a až pandemickému šíření chřipky v sezóně. Tyto faktory vedou k využití principů „reverzní vakcinologie“ a rekombinantních technologií pro vývoj nového typu vakcín.
Rekombinantní vakcíny a adjuvans
Využití poznatků virologie, molekulární biologie a rekombinantních technologií pro expresi proteinů v tkáňových kulturách otevřelo cestu k vývoji rekombinantních vakcín na bázi proteinů, anebo nově na bázi samo se replikujících mRNA vakcín. Na jedné straně se tento přístup vyznačuje možností rychlejšího vývoje vakcín a masovější produkcí vakcín, na druhé straně se jedná o sofistikované technologie a nutnost pokročilejší formulace vakcín (zejména mRNA vakcín) s použitím adjuvans. Vzhledem k faktu, že výběr adjuvans pro klinické použití pro humánní a veterinární aplikace je velmi omezen, probíhá současně vývoj nových adjuvans a celých systémů pro formulaci rekombinantních vakcín. Klasická adjuvans jsou založená na hydroxidu hlinitém nebo na olejových emulzích. Tato adjuvans mají omezené použití (např. hydroxid hlinitý u prasat) a nelze je použít pro mukózní imunizace. Nová adjuvans jsou založena na molekulárních adjuvans (např. monoforforyl lipid A) a biokompatibilních nanočásticích (např. liposomy, virosomy a částice podobné virum /VLP/, ISCOM). Využití těchto nových systémů a jejich kombinací je předmětem intenzivního výzkumu (probíhá i v ČR) s cílem optimalizovat imunitní odpověď.
Rekombinantní proteinové vakcíny jsou zaměřeny na proteinové konstrukty odvozené z hemaglutininu a neuraminidázy, které jsou připraveny metodami proteinového inženýrství a exprimovány v eukaryotických expresních systémech (savčí buňky, bakulovirové expresní systémy v hmyzích buňkách). Nejčastěji používanými savčími expresními systémy jsou buněčné linie MDCK a Vero.
Samostatnou kapitolu představují vakcíny na bázi messengerové mRNA. Předchůdcem genetických vakcín na bázi konstruktů nukleových kyselin kódujících antigeny, byly DNA vakcíny. Tyto vakcíny využívaly pDNA, což potenciálně kolidovalo s možností genové modifikace recipientů vakcíny a naráželo na předpisy o GMO. mRNA vakcíny nabízí výhody ve srovnání s DNA vakcínami z hlediska bezpečnosti. mRNA konstrukty obsahují pouze sekvence nukleotidů potřebné pro expresi proteinů, jsou rychle degradovány a neintegrují se do hostitelského genomu. Intradermální mRNA vakcína kódující celý gen PR8 H1 chránila mladé i staré myši proti letální infekci viry N1H1, H3N2 a H5N1. Stejná vakcína chránila prasata a snižovala šíření viru do prostředí (Petsch et al., 2012).
Modifikovaná mRNA vakcína kódující HA z viru H7N9 formulovaná v lipidních nanočásticích indukovala robustní imunitní odpověď v myších, fretkách a nižších primátech. Imunitní odpověď byla protektivní proti letální dávce viru (Bahl et al., 2017). Ta stejná vakcína byla bezpečná a imunogenní u lidí, jak prokázala randomizovaná studie fáze 1 (Bahl et al., 2017).
Vakcíny na bázi samo se replikujících mRNA tyto překážky překonávají a jejich komparativní výhodou proti proteinovým rekombinantním vakcínám je rychlost vývoje a výroby. Firma GSK předpokládá zhruba týdenní cyklus od identifikace genomu nového chřipkového viru až po výrobu dostatečného množství mRNA vakcíny po celém světě. To v principu dává možnost čelit propuknutí pandemií. Souběžně s touto novou technologií probíhá vývoj formulace mRNA vakcín a způsobu jejich aplikace (invazivní injekční, neinvazivní mukózní).
Možnost vývoje universální vakcíny proti chřipce je cílem výzkumu a vývoje předních vědeckých pracovišť (Daniela S. Rajão and Daniel R. Pérez 2018)
Úspěšná kontrola chřipkových infekcí je možná pouze za spolupráce mezi humánní a veterinární sférou. Snaha o vývoj široce protektivní vakcíny musí brát v potaz komplexní ekologii IAV a schopnost virů chřipky infikovat různé zvířecí druhy a člověka. Vyvinutá vakcína by měla být použitelná pro různé druhy zvířat a měla by být snadno dosažitelná v dostatečném množství pro použití při různých epidemiologických scénářích jako například během chřipkové sezóny. Platforma, na které je vyvinuta vakcína, by měla umožňovat masivní produkci, standardizaci pro potřeby registrace a možnost licencování výrobcům v jednotlivých regionech.
Influenza u prasat
Chřipkové virové onemocnění zůstává stále jednou z největších hrozeb pro lidské zdraví. Chřipka postihuje širokou škálu živočišných druhů a v ekologii chřipky hrají prasata důležitou roli. Význam prasat v etiologii chřipky spočívá v jejich náchylnosti k infekci různými viry influenzy, jako jsou viry chřipky ptáků a člověka. Při napadení prasete různými druhy chřipky může dojít ke vzniku reasortantů a ke vzniku nových typů virů, což vede k jevu zvanému antigenní posun (antigenic shift).
Chřipkový virus A (IAV) patří mezi nejvíce zničující patogeny vepřů a drůbeže. Několik geneticky a antigenně rozmanitých kmenů IAV je rozšířených ve světě a přetrvává jejich endemický výskyt. Infekce IAV způsobují významné ztráty v chovech prasat a to obvykle v důsledku snížených přírůstků hmotnosti, náchylnosti k sekundárním infekcím a vyvolání sporadických potratů spojených s hypertermií. U prasat má infekce IAV podobné vlastnosti jako nemoc u lidí. Vyznačuje se rychlým nástupem horečky, letargií, ztrátou chuti k jídlu a kašlem (Van Reeth et al., 2009 a 2012). Viry ptačí chřipky jsou endemické ve velkých částech světa, zejména v Asii, na Středním východě a v části Afriky (Světová zdravotnická organizace / Světová organizace pro zvířata Organizace pro zdraví, výživu a zemědělství (WHO / OIE / FAO) H5N1 Evolution Working Group, 2014).
Prasata lze z těchto důvodů označit jako „bioreaktory“ pro generování nových kmenů virů influenzy. Pro tuto roli „bioreaktorů“ lze uvést tři podpůrné argumenty: (1) prasata jsou citlivá na ptačí a lidské viry; (2) reasortované viry vzniklé přeskupením segmentů RNA z virů prasat, ptáků a lidí se vyskytují u prasat a (3) prasata mohou přenášet reasortované viry na lidi (Ma et al., 2009). Infekce prasat reasortanty by však mohla mít za následek vznik virů adaptovaných na prasata, což je nezbytná podmínka pro udržení infekce ve stádech prasat, která tak představují další rezervoár virů pro potenciální přenos na člověka (Londt et al., 2012). Z těchto důvodů má prasečí chřipka význam jak pro veterinární, tak pro humánní medicínu. Příkladem jsou pandemie chřipky v roce 1957, 1968 a 2009, které byly způsobeny reasortanty virů vzniklých v prasatech (Fouchier et al., 2003; Garten et al., 2009).
Po pandemii chřipky H1N1 v roce 2009 způsobené virem, který má původ v prasečím viru, došlo k posunu výzkumných priorit v „influenzologii“. Výzkum se zaměřil na zlepšení znalostí o imunitní odpovědi u prasat infikovaných virem chřipky. Tato tendence má dva hlavní důvody: zaprvé, prase je významné hospodářské zvíře a je zdrojem viru chřipky, který může být adaptován na člověka; zadruhé, prase představuje vynikající zvířecí model pro studium různých mikrobiálních infekčních chorob a jejich imunoprofylaxe pomocí vakcinace. Podobnost prasečího a lidského imunitního systému z hlediska anatomie, fyziologie a genetiky pasuje prase do role zlatého standardu in vivo animálního modelu v imunologii. Pro studium infekce virem influenzy a pro testování vakcín jsou dostupné také další zvířecí modely, jako například model průběhu nemoci na fretkách a morčatech (Belser et al., 2011; Sun et al., 2010). Prasečí model infekce ovšem poskytuje lepší predikci účinku vakcín a léků na člověka než animální modely, které využívající malé hlodavce (Meurens et al., 2012).
V Evropě je chřipka prasat považována za jeden z nejdůležitějších primárních patogenů respiračního onemocnění prasat a infekce je primárně způsobena viry H1N1, H1N2 a H3N2 chřipky typu A. Antigenní vlastnosti těchto virů je odlišují od ostatních cirkulujících virů influenzy prasat v jiných částech světa. Tyto viry zůstaly endemické v evropských populacích prasat, ale významné rozdíly v cirkulaci těchto kmenů se vyskytují na regionální úrovni v celé Evropě. Ke komplexní epidemiologii přispívá dynamika společné cirkulace virů, vliv předchozí imunity, chovatelské postupy a další lokální faktory. Programy sledování virů influenzy u evropských prasat neodhalily přítomnost pandemického viru H1N1 před jeho detekcí u lidí v roce 2009, existuje však důkaz, že virus může přežívat v evropských chovech prasat, i když existuje relativně dobrá úroveň odolnosti stáda vůči jiným virům H1 (Brown, 2013).
Chřipka je faktorem, který přispívá k chronickému respiračnímu onemocnění prasat kvůli možné koinfekci dvěma nebo více respiračními patogeny. Chřipková infekce je také spojena s potratem vyvolaným horečkou u prasnic. Chřipkový virus napadá epitelové buňky nosní sliznice, mandlí, průdušnice a plíce. Epitelové buňky průdušek, bronchiolů a alveol mohou v důsledku infekce a zánětu nekrotizovat, což vede k obstrukci dýchacích cest. Stejně závažný je výskyt subklinických infekcí, kdy se mohou prasata nakazit jedním nebo více chřipkovými podtypy bez zjevných příznaků nemoci. Jak již bylo naznačeno výše, zvýšená diverzita chřipkového viru u prasat je dána kombinací mechanismů založených na segmentovém přeskupení genů, na vzniku bodových mutací a na vzniku reasortantů při výměně segmentů RNA od jiných chřipkových virů, zejména těch od lidí. Jakmile dojde ke vzniku nového viru, nastartuje se vysoce dynamický proces adaptace prostřednictvím uvedených mechanismů a v populaci prasat se dále vyvíjí nové varianty s těžko předvídatelným infekčním potenciálem. (Nelson et al 2015). Vzhledem k možnému přenosu chřipkových virů z člověka, koní a ptáků na prasata, jeví se profylaxe u prasat jako jedno ze základních opatření namířených proti vzniku nových pandemií chřipky. Chov vepřů je vzhledem ke globalizaci světové ekonomiky zdrojem možného zavlečení různých kmenů virů chřipky mezi kontinenty. Vakcinační strategie má zásadní význam pro potlačení epidemie chřipky jak u lidí, tak u hospodářských zvířat. Vývoj virů chřipky na americkém kontinentě, v Evropě a v Asii je sumarizován v práci publikované (Vincent AL et al. 2017).
V ČR je dostupná inaktivovaná vakcína RESPIPORC FLU3, která obsahuje 3 různé kmeny viru A chřipky prasat, které byly dříve inaktivovány (usmrceny). Přípravek RESPIPORC FLU3 je injekční suspenze. Použití přípravku RESPIPORC FLU3 u prasat zmírňuje klinické příznaky a snižuje počet virů v plicích po infekci způsobené virem A chřipky prasat. Výbor pro veterinární léčivé přípravky (CVMP) dospěl k závěru, že přínosy přípravku RESPIPORC FLU3 převyšují rizika vakcinace prasat od věku 56 dnů a starších a březích prasnic proti chřipce způsobené podtypy H1N1, H3N2 a H1N2, vedou ke snížení klinických příznaků a zátěže plic virem po infekci a doporučil, aby přípravku RESPIPORC FLU3 bylo uděleno rozhodnutí o registraci. Evropská komise udělila rozhodnutí o registraci přípravku RESPIPORC FLU3 platné v celé Evropské unii společnosti IDT Biologika GmbH dne 14/01/2010. (https://www.ema.europa.eu/en/documents/overview/respiporc-flu3-epar-summary-public_cs.pdf)
Další vakcínou registrovanou v ČR je přípravek Gripork španělské firmy LABORATORIOS HIPRA, S.A. Jedná se o inaktivovanou vakcínu s olejovým adjuvans, která obsahuje inaktivované viry kmenů chřipky A (Hsw1N1)OLL, (Hsw3N2)G a (Hsw3N2)SH.
Influenza u koní
Koně patří mezi velmi cenná hospodářská zvířata, která jsou ohrožována chřipkou. K dnešnímu dni byla na celém světě hlášena ohniska koňské chřipky s výjimkou malého počtu ostrovních států včetně Nového Zélandu a Islandu. Chřipka je endemická v Evropě a Severní Americe a je považována za potenciálně významný ekonomický faktor pro chov koní na celém světě. Dovoz vakcinovaných koní, kteří mohou být infikováni bez klinických příznaků, spolu s nedostatečnými karanténními postupy vedl k vypuknutí chřipkové infekce a vzniku několika závažných ohnisek. Například v Austrálii (2007), kdy bylo infikováno více než 76 000 koní ve více než 10 000 chovech (A.Cullinane and J.R.Newton Veterinary Microbiology,2013,167, 205-214). V současné době cirkuluje v chovech koní virus typu H3N8. (Daly et al. 2011). Vakcinace koní proti influenze je klíčovým přístupem k ochraně stád. Různé vakcinační strategie pro prevenci influenzy jsou shrnuty v přehledném článku publikovaném Palliotem a spoluautory (Paillot et al., 2006). Přes rozsáhlé používání vakcín k ochraně stád koní dochází k ohniskovým vypuknutím infekce. V roce 2003 došlo k rozsáhlému výskytu chřipky u vakcinovaného stáda dostihových koní ve městě Newmarket ve Velké Británii (Newton et al., 2006; Barquero a kol., 2007). Pravidelné vypuknutí chřipkových infekcí koní jsou od roku 2003 hlášeny ve Velké Británii, v dalších státech EU a v USA (Damiani et al., 2008; Barbic et al., 2009; Bryant et al., 2009, Bryant et al. 2010). Také v dalších regionech, které ne příliš často hlásí infekce koňskou chřipkou, jsou od roku 2003 hlášena propuknutí infekce. V Jižní Africe došlo k druhému propuknutí infekce na přelomu roku 2003-2004. Toto vzplanutí navazovalo na předchozí infekci z roku 1986/1987 v důsledku nedodržování bezpečnostních protokolů. (Guthrie et al., 1999; Guthrie, 2006).
Podobné propuknutí infekce bylo hlášeno v roce 2008 z Indie (Virmani et al., 2010). V roce 2007 byla ohniska infekce v Austrálii, která byla prosta koňské chřipky. I zde byly příčiny vypuknutí infekce v nedodržování bezpečnostních opatření, konkrétně nedodržování karanténní doby pro koně dovezené z Japonska (Callinan, 2008; Bryant et al., 2009).
Skrytým nebezpečím u koňské chřipky je možnost přenosu na psy, jak se ukázalo ve Velké Británii, v USA a Austrálii. Tento přenos může nastat jak konzumací potravy pro psy vyrobené z masa infikovaných koní, tak přímo kapénkovou nákazou psů, kteří jsou chováni spolu s koňmi. (Daly et al., 2008). Koně mohou být také článkem v přenosu ptačí chřipky z infikovaných divokých ptáků na psy a prasata. (Crawford et al 2005; Gorman et al., 1991)
Influenza u drůbeže
V roce 2006 schválila Evropská komise Francii a Nizozemsku vakcinační plány na preventivní očkování drůbeže proti vysoce patogennímu viru ptačí chřipky. Vakcinovat se budou pouze určité druhy ptáků v daných regionech. Francie začala očkovat drůbež
Francie přistoupila k masivnímu očkování drůbeže proti viru ptačí chřipky v pásu atlantického pobřeží na jihozápadě země, kde jsou migrační cesty divokých ptáků, kteří by mohli nakazit domácí drůbež. Po očkování se musí chovy velmi pečlivě sledovat a kontrolovat, aby se zamezilo nebezpečí propuknutí chřipky u očkovaných ptáků, vzhledem k tomu, že příznaky nákazy u vakcinovaných ptáků nejsou typické a infekce může probíhat skrytě a infikovaní ptáci mohou dál šířit virus. V České republice by připadala v úvahu jen vakcinace nouzová (tj. v případě přímého ohrožení) a jen v oblastech, v nichž by se nákaza objevila. Očkovali by se ptáci chovaní v zoologických zahradách, popřípadě geneticky cenné chovy. Vakcinace snižuje množství virů, které v prostředí šíří ptáci infikovaní ptačí chřipkou, čímž se snižuje infekční tlak na zbytek populace. Francie a Nizozemsko praktikují preventivní vakcinace drůbeže, ale jiné státy jako například Velká Británie tento krok kritizují s poukazem na možnost, že vakcinace příznaky nemoci zakryje a nezastaví šíření viru.
Současné vakcíny vyžadují pro efektní prevenci infekce podání tří dávek vakcíny, což je v poměrech EU pro vakcinaci drůbeže velmi obtížně realizovatelné. Kromě toho je nutné očkované ptáky pečlivě sledovat a provádět v chovech další kontroly (výtěry, krevní testy). Vakcinace a administrativa s ní spojená je velmi drahá a vysoké náklady si vyžádá i následné monitorování a kontrola chovů.
U drůbeže jsou v EU dva režimy vakcinace - nouzová a preventivní. Nouzovou vakcinaci mohou členské státy použít v případě, že se nákaza vysoce patogenním virem chřipky objeví na jejich území nebo v jeho těsné blízkosti. Je to krátkodobé opatření k potlačení propuknutí chřipky u drůbeže nebo u jiných vnímavých ptáků nebo pro zastavení šíření onemocnění z jiných oblastí, kde se již jeho výskyt potvrdil. Nouzové vakcinaci musí předcházet odhad rizika, z něhož je zřejmá míra nebezpečí.
Preventivní vakcinace je dlouhodobé opatření, které mohu členské státy zavést, pokud se obávají, že určitá drůbež nebo ptáci žijící v zajetí na jistých místech jsou více vystaveni riziku nákazy ptačí chřipkou a propuknutí nemoci. Oba druhy vakcinace musí proběhnout stejným způsobem a musí podléhat stejným pravidlům i přísnému dozoru a kontrole očkovaných ptáků.
Dalším aspektem vakcinace drůbeže je možnost přenosu infekce na ošetřovatele, kteří pracují v úzkém kontaktu s očkovanými ptáky, neboť zde hrozí riziko onemocnění virem H5N1. I to je důvod pro pečlivý monitoring vakcinovaných chovů a testování přítomnosti viru.
Ekonomické hledisko preventivní vakcinace drůbeže je rozhodující z hlediska vývoje moderních vakcín. Kombinace vakcíny, která by měla ideálně být aplikována v jedné dávce, spolu s vhodnou technologií pro levnou masovou vakcinaci drůbeže, je určujícím faktorem pro vývoj moderních vakcín. Společnost Embrex založená v roce 1985 vyvinula zařízení Inovoject System, pomocí kterého je vakcína aplikována přímo do vajíček, ve kterých se vyvíjejí kuřecí embrya. Tato in ovo vakcinace odstraňuje finančně i časově nákladnou ruční vakcinaci jednodenních kuřat v líhních. Moderní rekombinantní vakcíny založené na samo se replikujících mRNA konstruktech jsou potenciálně vhodné pro kombinování s in ovo vakcinací. Nabízí se možnost spojit vakcinaci proti chřipce s vakcinací proti Newcastelské nemoci drůbeže pomocí samo se replikujících mRNA vakcín a in ovo aplikace. Výzkum a vývoj v této oblasti by měl být podpořen v projektech agrárního výzkumu MZe.
Možnosti vývoje a výroby moderních vakcín v České republice
V současné době jsou v České republice dva výrobci vakcín, kteří disponují výrobní infrastrukturou pro výrobu pokročilejších typů vakcín a tuto infrastrukturu rozvíjejí. Jedná se o firmu Bioveta, a.s. Ivanovice na Hané a Dyntec Terezín. Obě tyto firmy mají také svoji vývojovou základnu, které ovšem není dostačující a neobejdou se bez spolupráce s univerzitami a s výzkumnými ústavy.
Nejkomplexnější přístup k vývoji vakcín nabízí Výzkumný ústav veterinárního lékařství, v.v.i. Brno (VUVeL), kde je moderní infrastruktura nutná pro vývoj nejpokročilejších vakcín. Tato infrastruktura byla vybudována v rámci OPVVV projektů FIT, CEREBIT a IMUNOFARMAKOTERAPIE. Současná moderní vakcinologie je založena na komplexním přístupu mnoha vědních oborů, zejména imunologie, organické chemie a materiálového výzkumu. Spolupráce na této tématice probíhá v koordinovaném úsilí pracovníků VÚVeL, Univerzity Palackého v Olomouci, VŠCHT Praha, TU Liberec. Syntetické chemické komponenty pro moderní vakcíny (např. molekulární adjuvans) jsou pro potřeby výzkumu syntetizovány pražskou firmou Apigenex. Tato spolupráce již v minulosti vedla k vývoji originálních molekulárních adjuvans, lipidů pro přípravu nosičů vakcín a nanovlákenných materiálů pro mukoadhezivní filmy využívané k vývoji mukózních vakcín vhodných pro neinvazivní vakcinace, zejména proti chřipce.
Česká republika tedy disponuje nezbytnou kvalitou výzkumu a průmyslu pro vývoj moderních vakcín a další rozvoj farmaceutického průmyslu v oblasti imunofarmak a vakcín. Tento segment farmakologického globálního trhu je nejdynamičtěji se rozvíjejícím s nárůstem kolem 13%. Také z hlediska exportního potenciálu, zejména do agrárního sektoru, je produkce vakcín perspektivním odvětvím, pro které v České republice existují veškeré předpoklady. Jednotlivé platformy pro vývoj vakcín proti chřipce jsou na obrázku 3. Pro vývoj všech těchto platforem jsou v ČR odpovídající infrastruktury a odborníci.

Obr. 3. Schematické znázornění jednotlivých platforem pro vývoj vakcíny proti chřipce
(Rajão D.S. and Pérez DR. Universal Vaccines and Vaccine Platforms to Protect against Influenza Viruses in Humans and Agriculture. Frontiers in Microbiology 2018, 9 doi: 10.3389/fmicb.2018.00123)
Literatura
Bahl, K., Senn, J. J., Yuzhakov, O., Bulychev, A., Brito, L. A., Hassett, K. J., et al. (2017). Preclinical and clinical demonstration of immunogenicity by mRNA vaccines against H10N8 and H7N9 influenza viruses.Mol. Ther. 25, 1316–1327. doi: 10.1016/j.ymthe.2017.03.035
Barquero, N., Daly, J.M., Newton, J.R., 2007. Risk factors for influenza infection in vaccinated racehorses: lessons from an outbreak in Newmarket, UK in 2003.Vaccine 25, 7520–7529.
Belser, J.A., Katz, J.M., Tumpey, T.M., 2011. The ferret as a model organism to study influenza A virus infection. Disease Models and Mechanisms 4, 575–579.
Brown IH. History and epidemiology of Swine influenza in Europe. Curr Top Microbiol Immunol. 2013; 370:133-46.
Bryant, N.A., Paillot, R., Rash, A.S., Medcalf, E., Montesso, F., Ross, J., Watson, J., Jeggo, M., Lewis, N.S., Newton, J.R., Elton, D.M., 2010. Comparison of two modern vaccines and previous influenza infection against challenge with an equine influenza virus from the Australian 2007 outbreak. Veterinary Research 2007, 41, 19.
Bryant, N.A., Rash, A.S., Russell, C.A., Ross, J., Cooke, A., Bowman, S., MacRae, S., Lewis, N.S., Paillot, R., Zanoni, R., Meier, H., Griffiths, L.A., Daly, J.M., Tiwari, A., Chambers, T.M., Newton, J.R., Elton, D.M., 2009. Antigenic and genetic variations in European and North American equine influenza virus strains (H3N8) isolated from 2006 to 2007. Veterinary Microbiology 2010, 138, 41–52.
Callinan, I., 2008. Equine Influenza: The August 2007 Outbreak in Australia. Report of the Equine Influenza Inquiry. The Commonwealth of Australia. <http:// www.equineinfluenzainquiry.gov.au/eiiexhibits/REP.0001.001.0001
Crawford, P.C., Dubovi, E.J., Castleman, W.L., Stephenson, I., Gibbs, E.P., Chen, L., Smith, C., Hill, R.C., Ferro, P., Pompey, J., Bright, R.A., Medina, M.J., Johnson, C.M., Olsen, C.W., Cox, N.J., Klimov, A.I., Katz, J.M., Donis, R.O. Transmission of equine influenza virus to dogs. Science 2005, 310, 482–485.
Crisci E et al. Influenza virus in pigs. Molecular Immunology 2013, 55, 200– 211.
Damiani, A.M., Scicluna, M.T., Ciabatti, I., Cardeti, G., Sala, M., Vulcano, G., Cordioli, P., Martella, V., Amaddeo, D., Autorino, G.L.,. Genetic characterization of equine influenza viruses isolated in Italy between 1999 and 2005. Virus Research 2008, 131, 100–105.
Daly, J.M., Blunden, A.S., Macrae, S., Miller, J., Bowman, S.J., Kolodziejek, J., Nowotny, N., Smith, K.C., 2008. Transmission of equine influenza virus to English foxhounds. Emerging Infectious Diseases 14, 461–464.
Janet M. Daly, Shona MacRaeJ, Richard Newton, Eva Wattrang, Debra M. Elton. Equine influenza: A review of an unpredictable virus. The Veterinary Journal 2011,89, 7–14.
Fouchier, R.A., Osterhaus, A.D., Brown, I.H.,. Animal influenza virus surveillance. Vaccine 2003, 21, 1754–1757.
Garten, R.J., Davis, C.T., Russell, C.A., et al. Antigenic and genetic characteristics of swineorigin
2009 A(H1N1) influenza viruses circulating in humans. Science2009, 325, 197–201.
Gorman, O.T., Bean, W.J., Kawaoka, Y., Donatelli, I., Guo, Y., Webster, R.G., Evolution of influenza A virus nucleoprotein genes: implications for the origins of H1N1 human and classical swine viruses. Journal of Virology 1991, 65, 3704–3714.
Guthrie, A.J., 2006. Equine influenza in South Africa, 2003 outbreak. In: Proceedings of the 9th International Congress of World Equine Veterinary Association. International Veterinary Information Service.
Guthrie, A.J., Stevens, K.B., Bosman, P.P., The circumstances surrounding the outbreak and spread of equine influenza in South Africa. Scientific and Technical Review of the Office International des Epizooties 1999, 18, 179–185.
Londt, B.Z., Brookes, S.M., Nash, B.J., Nunez, A., Stagg, D.A., Brown, I.H., 2012. The infectivity of pandemic 2009 H1N1 and avian influenza viruses for pigs: an assessment by ex vivo respiratory tract organ culture. Influenza and Other Respiratory Viruses. 2013 May; 7(3):393-402 http://dx.doi.org/10.1111/j. 1750-2659.2012.00397.x
Meurens, F., Summerfield, A., Nauwynck, H., Saif, L., Gerdts, V., 2012. The pig: a model for human infectious diseases. Trends in Microbiology 20, 50–57.
Nelson M.I., Vincent, A.L., Reverse zoonosis of influenza to swine: new perspectives on the human-animal interface. Trends Microbiol. 2015, 23, 142–153
Newton, J.R., Daly, J.M., Spencer, L., Mumford, J.A., 2006. Description of the equine influenza (H3N8) outbreak in the United Kingdom during 2003, during which recent vaccination failed to prevent disease in racehorses in Newmarket. Veterinary Record 158, 185–192.
Paillot, R., Hannant, D., Kydd, J.H., Daly, J.M., 2006. Vaccination against equine influenza: quid novi? Vaccine 24, 4047–4061.
Petsch, B., Schnee, M., Vogel, A. B., Lange, E., Hoffmann, B., Voss, D., et al. (2012). Protective efficacy of in vitro synthesized, specific mRNA vaccines against influenza A virus infection. Nat. Biotechnol. 30, 1210–1216. doi: 10.1038/nbt.2436.
Rajão D.S. and Pérez DR. Universal Vaccines and Vaccine Platforms to Protect against Influenza Viruses in Humans and Agriculture. Frontiers in Microbiology 2018, 9 doi: 10.3389/fmicb.2018.00123
Sun, Y., Bi, Y., Pu, J., et al. Guinea pig model for evaluating the potential public health
risk of swine and avian influenza viruses. PLoS ONE 2010, 5, e15537.
Van Reeth, K., Braeckmans, D., Cox, E., Van Borm, S., van den Berg, T., Goddeeris,B., et al. (2009). Prior infection with an H1N1 swine influenza virus partially protects pigs against a low pathogenic H5N1 avian influenza virus. Vaccine 27, 6330–6339. doi: 10.1016/j.vaccine.2009.03.021
Van Reeth, K., Brown, I. H., and Olsen, C.W. (2012). “Influenza virus,” in Diseases of Swine, 10th Edn., eds J. J. Zimmerman, L. A. Karriker, A. Ramirez, K. J. Schwartz, and G.W. Stevenson (Ames, IA:Wiley-Blackwell), 557–571.
Vincent AL et al. Influenza A virus vaccines for swine. Veterinary Microbiology 2017, 206 35–44.
Virmani, N., Bera, B.C., Singh, B.K., Shanmugasundaram, K., Gulati, B.R., Barua, S., Vaid, R.K., Gupta, A.K., Singh, R.K., 2010. Equine influenza outbreak in India (2008–09): virus isolation, sero-epidemiology and phylogenetic analysis of HA gene. Veterinary Microbiology. doi:10.1016/j.vetmic.2009.12.007.
